陈时中还为台湾自产疫苗不做三期试验辩解 学者痛批不诚实
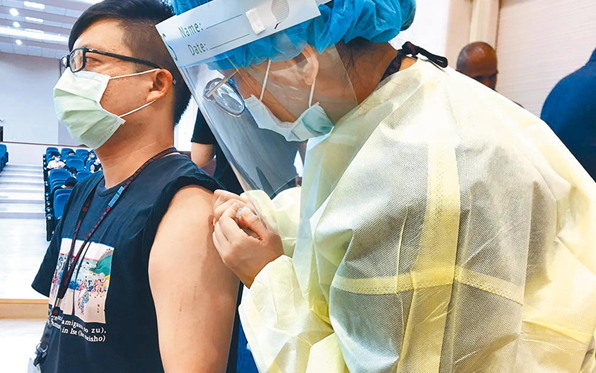
岛内亟需疫苗。(图片来源:台湾“中时新闻网”)
中国台湾网6月1日讯 据台湾《中国时报》报道,台湾自产疫苗未完成二期临床试验,台流行疫情指挥中心就与药厂签约,引发舆论质疑。该中心解释称,目前无论阿斯利康(AZ)、莫德纳还是BNT,通通都没完成第三期临床试验,且一、二期受试人数远小于台自产疫苗,因此给自产疫苗“紧急使用授权(EUA)”没有问题。台湾政治大学副教授刘宏恩痛批指挥中心大玩话术又不诚实。
陈时中声称,BNT疫苗预估2023年4月才完成第三期临床试验,莫德纳2022年10月完成三期临床,但世卫组织、美国、加拿大、英国、日本各自在去年及今年5月前核准。他称,台湾2家自产疫苗二期临床试验已收超过3800人,远高于AZ、莫德纳、BNT获“紧急使用授权”前仅数百人的二期临床人数。
刘宏恩指出,什么是话术?把“临床试验毋需第3期完全做完”讲成“临床试验毋需进行到第3期”,就叫话术;什么是诚实?明明并非比照美国食品药物管理局(FDA)国际标准来审查自产疫苗紧急许可,那就明白承认自己的标准比较宽松,不可以说自己的标准跟他们同样严格,否则就是不诚实。
他指出,BNT疫苗有临床试验第三期4.4万人受试数据;莫德纳有第三期约3万人、娇生有第三期约4.4万人、AZ也有第三期约2.4万人受试数据,才各获得美国食品药物管理局及欧盟同意其申请。他表示,去年10月台当局公告“自产疫苗紧急授权许可只需要做临床试验第二期,且受试者只需3000人以上”,他就非常担忧。请民进党当局务必讲清楚,为何采取比欧美宽松的标准?7个多月过去了,民众的信任愈来愈动摇,如今政策沟通与修正调整的时机早已错过,只能被口水淹没。(中国台湾网 李宁)



